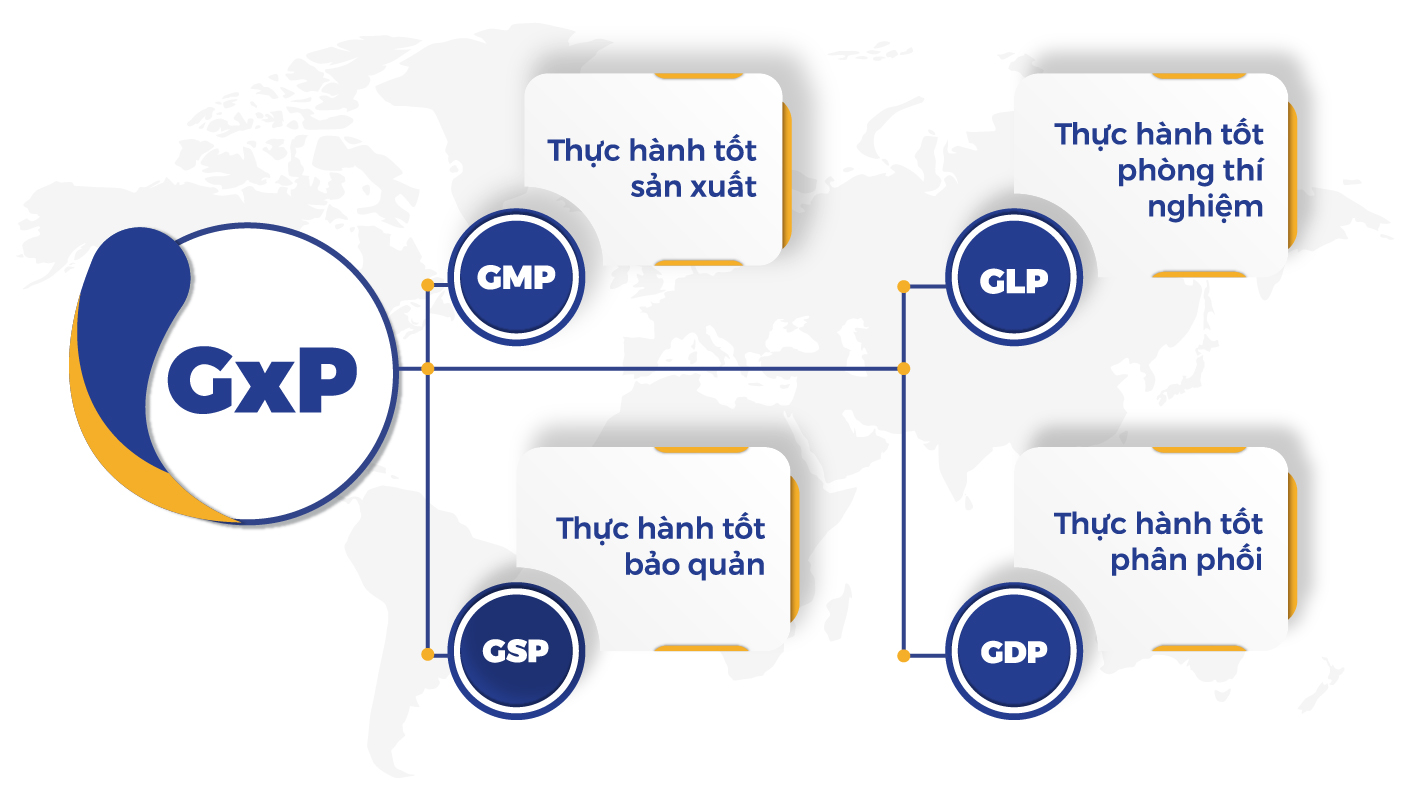
Hồ sơ thẩm định phòng sạch là gì?
Trong ngành dược phẩm, phòng sạch không chỉ là yêu cầu bắt buộc để đảm bảo an toàn sản phẩm, mà còn là điều kiện tiên quyết trong quá trình thẩm định theo tiêu chuẩn GMP. Để được phê duyệt và đưa vào vận hành, doanh nghiệp phải chuẩn bị đầy đủ hồ sơ thẩm định phòng sạch dược phẩm, bao gồm hệ thống kiểm soát môi trường, thiết bị và các minh chứng đánh giá vận hành.
Là đơn vị cung cấp thiết bị phòng sạch, VietnamCleanroom tổng hợp một bộ hồ sơ chuẩn giúp doanh nghiệp nắm rõ các yêu cầu cần chuẩn bị trước khi kiểm định GMP.
Hồ sơ thẩm định phòng sạch dược phẩm là bộ tài liệu chứng minh rằng khu vực sản xuất đáp ứng yêu cầu GMP về:
-
Thiết kế, xây dựng
-
Thiết bị, kiểm soát môi trường
-
Vận hành, quản lý rủi ro
-
Giám sát, kiểm tra đánh giá
Mục tiêu của hồ sơ thẩm định là chứng minh rằng phòng sạch dược phẩm có khả năng vận hành ổn định, kiểm soát được hạt bụi, vi sinh, áp suất và đảm bảo không gây nhiễm chéo cho sản phẩm.
>>> Xem thêm: Kiểm soát bụi mịn trong phòng sản xuất viên nén
Các phần chính trong hồ sơ thẩm định phòng sạch dược phẩm theo GMP
Hồ sơ thiết kế (DQ – Design Qualification)
Đây là bước đầu tiên, chứng minh rằng thiết kế đáp ứng tiêu chuẩn GMP.
Nội dung DQ gồm:
-
Mặt bằng và sơ đồ bố trí phòng sạch
-
Phân cấp độ sạch (ISO 5 – ISO 8 tùy khu vực)
-
Luồng người, luồng vật liệu
-
Vật liệu xây dựng, vật liệu hoàn thiện
-
Bản vẽ hệ thống HVAC, AHU, HEPA
-
Danh mục thiết bị phòng sạch sử dụng trong toàn bộ khu vực

Thẩm định lắp đặt (IQ – Installation Qualification)
IQ chứng minh hệ thống phòng sạch đã được lắp đặt đúng thiết kế.
Tài liệu IQ:
-
Biên bản kiểm tra lắp đặt thiết bị lọc HEPA/ULPA
-
Biên bản nghiệm thu AHU, chiller, hệ thống điều khiển
-
Danh sách thiết bị phòng sạch (Air Shower, Pass Box, đồng hồ chênh áp, FFU…)
-
Hồ sơ vật liệu: chứng nhận inox, panel PU, epoxy, kính cường lực…
-
Biên bản kiểm tra hướng gió, đường ống, điện, điều khiển

Thẩm định vận hành (OQ – Operational Qualification)
OQ xác minh rằng hệ thống hoạt động đúng theo thông số thiết kế.
Các kiểm tra OQ bao gồm:
-
Kiểm tra chênh áp giữa các phòng
-
Tốc độ gió tại vị trí FFU, LAF
-
Kiểm tra HEPA leak test
-
Kiểm tra ánh sáng, độ ồn, độ rung
-
Kiểm tra kích hoạt của Air Shower, interlock Pass Box
-
Kiểm tra hệ thống đo, giám sát môi trường (temperature, RH, particle counter)

Thẩm định hiệu năng (PQ – Performance Qualification)
Đây là bước quan trọng nhất để chứng minh phòng sạch đạt hiệu năng trong điều kiện sản xuất thực tế.
Nội dung PQ:
-
Kiểm tra nồng độ hạt bụi theo ISO (at-rest và in-operation)
-
Kiểm tra vi sinh trong không khí và bề mặt
-
Kiểm tra hiệu quả kiểm soát chênh áp trong suốt ca sản xuất
-
Theo dõi độ ẩm, nhiệt độ liên tục 24h/7
-
Đánh giá nguy cơ nhiễm chéo khi vận hành thực tế
-
Hồ sơ SOP vận hành, vệ sinh phòng sạch dược phẩm

Các thiết bị phòng sạch cần có trong hồ sơ thẩm định
Trong phòng sạch dược phẩm, thiết bị là một phần quan trọng của hồ sơ GMP.
Thiết bị phòng sạch đóng vai trò trung tâm trong việc đáp ứng tiêu chuẩn GMP. Các hệ thống lọc khí HEPA/ULPA, AHU, FFU, Air Shower, Pass Box, đồng hồ chênh áp, thiết bị monitoring bụi, độ ẩm, nhiệt độ và các thiết bị tiệt khuẩn đều phải được chứng minh có nguồn gốc rõ ràng, đạt chuẩn kỹ thuật và phù hợp với cấp độ sạch yêu cầu.
Tính đồng bộ của thiết bị phòng sạch không chỉ ảnh hưởng đến chất lượng hồ sơ thẩm định mà còn quyết định khả năng vận hành ổn định lâu dài của phòng sạch dược phẩm.
 |
 |
Quy trình chuẩn bị hồ sơ thẩm định phòng sạch dược phẩm
Quy trình chuẩn bị hồ sơ thẩm định đòi hỏi doanh nghiệp rà soát thiết kế, chuẩn hóa thiết bị, hoàn thiện bản vẽ kỹ thuật, lập kế hoạch thẩm định, tiến hành kiểm tra thực tế và lập báo cáo đầy đủ trước khi trình đơn vị chứng nhận GMP.
Trong suốt quá trình này, mọi dữ liệu đo kiểm phải được lưu trữ và minh bạch, đặc biệt các thông số về bụi, vi sinh và áp suất phải đạt chuẩn phân cấp phòng. Hồ sơ SOP vận hành và vệ sinh phòng sạch cũng là phần bắt buộc nhằm đảm bảo khả năng duy trì điều kiện sạch trong dài hạn.
>>> Xem thêm: Quy trình thẩm định thiết bị phòng sạch theo GMP trong ngành dược phẩm
Lưu ý quan trọng khi lập hồ sơ thẩm định phòng sạch
-
Tất cả thông số phải có nguồn gốc thiết bị rõ ràng
-
HEPA và AHU phải có chứng nhận test kèm theo
-
Kết quả đo bụi – vi sinh phải đạt yêu cầu phân cấp phòng
-
Hồ sơ SOP vận hành vệ sinh là bắt buộc
-
Tài liệu kiểm tra định kỳ phải được lưu trữ tối thiểu 5 năm
-
Thiết bị phòng sạch phải đồng bộ và phù hợp từng cấp độ sạch
Vietnam Cleanroom (VCR) là một doanh nghiệp hàng đầu tại Việt Nam chuyên cung cấp thiết bị và giải pháp phòng sạch. Với hơn 10 năm kinh nghiệm phục vụ các dự án phòng sạch đạt tiêu chuẩn GMP, VCR tự hào mang đến các thiết bị kỹ thuật cao như: đồng hồ chênh áp, khóa liên động, đèn phòng sạch, Pass Box, FFU (Fan Filter Unit), buồng cân, HEPA Box, Air Shower, cửa thép phòng sạch, tủ cách ly (ISOLATOR), và nhiều loại phụ kiện chuyên dụng khác
Không chỉ là nhà cung cấp thiết bị, VCR còn là đơn vị phân phối độc quyền các sản phẩm từ các thương hiệu quốc tế như LENGE và BLOCK Technical, đồng thời cung cấp các giải pháp phòng sạch toàn diện cho các lĩnh vực như dược phẩm, điện tử, y tế, thực phẩm và mỹ phẩm. VCR có đội ngũ chuyên gia giàu kinh nghiệm, kiến thức chuyên sâu về phòng sạch, hỗ trợ tư vấn về tiêu chuẩn, thiết kế, thi công và vận hành phòng sạch theo chuẩn ISO, GMP, HACCP, ISO 14644
VCR hướng đến trở thành thương hiệu quốc dân trong ngành phòng sạch, với mạng lưới cung ứng rộng khắp, VCR có các văn phòng tại Hà Nội, TP. HCM, đáp ứng mọi yêu cầu từ xây dựng đến nâng cấp môi trường sản xuất đạt chuẩn
Email: [email protected]
Điện thoại: (+84) 901239008
Địa chỉ:
VP Hà Nội: 9/675 Lạc Long Quân, P. Xuân La, Q. Tây Hồ, TP. Hà Nội
VP Hồ Chí Minh: 15/42 Phan Huy Ích, P.15, Q. Tân Bình, TP.HCM
Hãy liên hệ với VCR để tìm hiểu thêm về lĩnh vực phòng sạch hiệu quả nhất nhé!