- 1. Tổng quan về Validation Master Plan trong nhà máy dược
- 2. Cấu trúc tiêu chuẩn của một VMP
- 3. Các loại thẩm định trong VMP
- 4. Quy trình xây dựng Validation Master Plan
- 5. Yêu cầu GMP đối với Validation Master Plan
- 6. Ứng dụng VMP trong vận hành nhà máy dược
- 7. Vai trò của hệ thống phòng sạch trong VMP
- 8. Những lưu ý quan trọng khi xây dựng VMP
- 9. FAQ - Câu hỏi thường gặp về Validation Master Plan
- 10. Kết luận
Đây không chỉ là tài liệu định hướng cho toàn bộ hoạt động thẩm định mà còn là cơ sở để chứng minh với cơ quan quản lý rằng nhà máy được thiết kế, vận hành và kiểm soát đúng chuẩn. Việc Xây dựng Validation Master Plan (VMP) cho nhà máy dược GMP một cách bài bản ngay từ đầu sẽ giúp doanh nghiệp giảm rủi ro, tối ưu chi phí và sẵn sàng cho mọi đợt đánh giá GMP. Cùng VCR tìm hiểu thêm về Xây dựng VMP qua bài viết này.
1. Tổng quan về Validation Master Plan trong nhà máy dược
Trong ngành dược phẩm, việc kiểm soát chất lượng không chỉ dừng lại ở sản phẩm cuối cùng mà phải được đảm bảo xuyên suốt toàn bộ quá trình từ thiết kế, xây dựng đến vận hành nhà máy. Một trong những công cụ quan trọng giúp thực hiện điều này là Validation Master Plan (VMP - Kế hoạch thẩm định tổng thể). Đây là tài liệu mang tính chiến lược, định hướng toàn bộ hoạt động thẩm định nhằm đảm bảo rằng mọi hệ thống, thiết bị và quy trình đều hoạt động đúng như thiết kế và đáp ứng yêu cầu chất lượng.
Về bản chất, VMP là tài liệu cấp cao mô tả phạm vi, phương pháp và kế hoạch thực hiện các hoạt động thẩm định trong nhà máy dược. Nó không đi sâu vào chi tiết từng thử nghiệm mà đóng vai trò như “bản đồ tổng thể”, giúp doanh nghiệp xác định rõ những gì cần thẩm định, cách thức thực hiện và trình tự triển khai. Một VMP được xây dựng tốt sẽ giúp đồng bộ các hoạt động validation, tránh chồng chéo, thiếu sót và đảm bảo mọi hạng mục quan trọng đều được kiểm soát.
Vai trò của VMP trong hệ thống chất lượng dược phẩm là rất quan trọng. Đây là cầu nối giữa yêu cầu pháp lý và thực tế vận hành, giúp doanh nghiệp chứng minh rằng toàn bộ hệ thống sản xuất được kiểm soát chặt chẽ. VMP không chỉ hỗ trợ việc lập kế hoạch mà còn giúp quản lý rủi ro, tối ưu nguồn lực và đảm bảo tính nhất quán trong quá trình thẩm định. Trong các đợt thanh tra hoặc đánh giá GMP, VMP thường là một trong những tài liệu đầu tiên được xem xét để đánh giá mức độ tuân thủ của nhà máy.
Mối liên hệ giữa VMP và GMP là rất chặt chẽ. GMP yêu cầu tất cả các hệ thống ảnh hưởng đến chất lượng sản phẩm phải được thẩm định và chứng minh hiệu quả. VMP chính là công cụ giúp doanh nghiệp đáp ứng yêu cầu này một cách có hệ thống. Thông qua VMP, các hoạt động thẩm định như thiết bị, quy trình sản xuất, hệ thống HVAC hay hệ thống tiện ích đều được lập kế hoạch và triển khai theo đúng chuẩn. Nói cách khác, VMP là nền tảng giúp chuyển các nguyên tắc GMP thành hành động cụ thể trong nhà máy.
Không phải ngẫu nhiên mà VMP được xem là tài liệu bắt buộc trong nhà máy dược. Việc thiếu VMP hoặc xây dựng không đầy đủ có thể dẫn đến nhiều rủi ro như bỏ sót các hạng mục cần thẩm định, thực hiện không nhất quán hoặc không có cơ sở chứng minh khi bị kiểm tra. Trong môi trường sản xuất dược phẩm, nơi mọi sai sót đều có thể ảnh hưởng đến sức khỏe người dùng, việc có một VMP rõ ràng, đầy đủ và cập nhật là yêu cầu không thể thiếu.
Các hoạt động thẩm định trong VMP rất đa dạng và bao phủ toàn bộ hệ thống nhà máy. Điều này bao gồm thẩm định thiết bị (qualification), thẩm định quy trình sản xuất, thẩm định làm sạch, thẩm định hệ thống HVAC và thẩm định các hệ thống tiện ích như nước tinh khiết, khí nén hoặc hơi sạch. Ngoài ra, trong bối cảnh số hóa, thẩm định hệ thống máy tính (Computer System Validation - CSV) cũng ngày càng trở nên quan trọng. Mỗi hoạt động đều có vai trò riêng nhưng đều hướng đến mục tiêu chung là đảm bảo hệ thống vận hành ổn định, nhất quán và tạo ra sản phẩm đạt chất lượng.
Nhìn chung, Validation Master Plan không chỉ là một tài liệu mang tính hình thức mà là nền tảng cốt lõi của hệ thống chất lượng trong nhà máy dược. Việc xây dựng VMP bài bản ngay từ đầu sẽ giúp doanh nghiệp kiểm soát tốt toàn bộ hoạt động thẩm định, giảm thiểu rủi ro và sẵn sàng đáp ứng các yêu cầu kiểm tra từ cơ quan quản lý.
Xem thêm: Commissioning và Validation phòng sạch giống hay khác nhau?
2. Cấu trúc tiêu chuẩn của một VMP
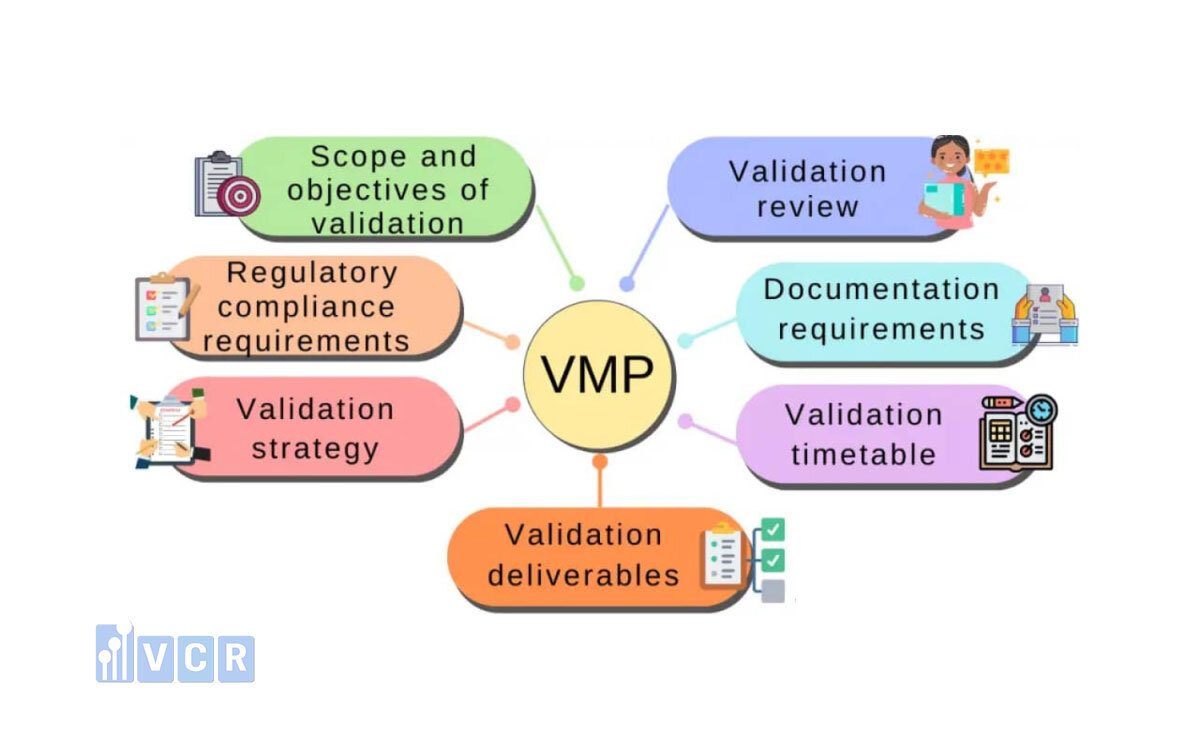
Một Validation Master Plan (VMP - Kế hoạch thẩm định tổng thể) đạt chuẩn không chỉ cần đầy đủ nội dung mà còn phải được xây dựng theo cấu trúc logic, rõ ràng và dễ truy xuất. Cấu trúc này giúp đảm bảo mọi hoạt động thẩm định được triển khai có hệ thống, tránh thiếu sót và đáp ứng yêu cầu của GMP cũng như các cơ quan quản lý.
Thành phần đầu tiên và quan trọng là phạm vi áp dụng (scope). Phần này xác định rõ VMP áp dụng cho khu vực nào, hệ thống nào và giai đoạn nào của nhà máy. Ví dụ, VMP có thể bao phủ toàn bộ nhà máy hoặc chỉ một khu vực sản xuất cụ thể. Việc xác định phạm vi rõ ràng giúp tránh nhầm lẫn và đảm bảo tất cả các hạng mục quan trọng đều được đưa vào kế hoạch thẩm định.
Tiếp theo là phần mô tả nhà máy và hệ thống. Đây là nội dung cung cấp cái nhìn tổng quan về cơ sở sản xuất, bao gồm sơ đồ nhà máy, các khu vực chức năng, hệ thống HVAC, hệ thống nước, khí và các dây chuyền sản xuất chính. Mục đích của phần này là giúp người đọc hiểu được bối cảnh vận hành và các yếu tố ảnh hưởng đến chất lượng sản phẩm, từ đó làm cơ sở cho việc lập kế hoạch thẩm định phù hợp.
Chính sách thẩm định (validation policy) là phần thể hiện quan điểm và định hướng của doanh nghiệp đối với hoạt động validation. Nội dung này thường bao gồm nguyên tắc thực hiện thẩm định, tiêu chí chấp nhận, phương pháp tiếp cận (risk-based approach) và mức độ kiểm soát cần thiết. Một chính sách rõ ràng sẽ giúp đảm bảo tính nhất quán trong toàn bộ hoạt động thẩm định và là cơ sở để đưa ra quyết định trong các tình huống phát sinh.
Một phần không thể thiếu trong VMP là danh mục thiết bị và hệ thống cần thẩm định. Danh mục này liệt kê chi tiết tất cả các thiết bị, quy trình và hệ thống có ảnh hưởng đến chất lượng sản phẩm, chẳng hạn như máy móc sản xuất, hệ thống HVAC, hệ thống nước tinh khiết, hệ thống khí nén và phần mềm điều khiển. Việc lập danh mục đầy đủ giúp đảm bảo không bỏ sót bất kỳ hạng mục nào cần thẩm định, đồng thời hỗ trợ việc theo dõi tiến độ thực hiện.
Kế hoạch và lịch trình thực hiện là phần chuyển hóa chiến lược thành hành động cụ thể. Nội dung này bao gồm timeline (lịch trình), thứ tự thực hiện các hoạt động thẩm định và phân bổ nguồn lực. Một kế hoạch hợp lý cần cân đối giữa tiến độ dự án và khả năng thực hiện, tránh tình trạng chậm trễ hoặc quá tải. Ngoài ra, việc xác định rõ các mốc quan trọng (milestones - cột mốc) sẽ giúp kiểm soát tiến độ và đánh giá hiệu quả triển khai.
Vai trò và trách nhiệm của các bên liên quan cũng cần được xác định rõ trong VMP. Các bộ phận như QA, QC, kỹ thuật và sản xuất đều có vai trò nhất định trong quá trình thẩm định. Việc phân công rõ ràng giúp tránh chồng chéo, đảm bảo mỗi công việc đều có người chịu trách nhiệm và tăng tính minh bạch trong quá trình thực hiện.
Cuối cùng, hệ thống tài liệu và kiểm soát thay đổi là yếu tố đảm bảo tính bền vững của VMP. Tất cả các tài liệu liên quan đến thẩm định cần được quản lý theo hệ thống kiểm soát tài liệu (document control), đảm bảo dễ truy xuất và cập nhật. Bên cạnh đó, mọi thay đổi liên quan đến thiết bị, quy trình hoặc hệ thống đều phải được đánh giá và phê duyệt thông qua quy trình kiểm soát thay đổi (change control). Điều này giúp duy trì tính nhất quán và đảm bảo rằng mọi thay đổi đều không ảnh hưởng tiêu cực đến chất lượng sản phẩm.
Trong thực tế, việc xây dựng một VMP hoàn chỉnh đòi hỏi sự phối hợp giữa nhiều bộ phận và kinh nghiệm chuyên môn sâu. Đặc biệt, các hệ thống phòng sạch và HVAC - yếu tố quan trọng trong nhà máy dược - cần được tích hợp chặt chẽ vào cấu trúc VMP. Các đơn vị như Thiết bị phòng sạch VCR có thể hỗ trợ cung cấp thiết bị và giải pháp phù hợp, giúp đảm bảo các hạng mục liên quan đến môi trường sản xuất được thẩm định đúng chuẩn.
Tóm lại, cấu trúc của một VMP không chỉ là danh sách các nội dung cần có mà còn là khung xương giúp toàn bộ hoạt động thẩm định được triển khai một cách khoa học, hiệu quả và tuân thủ GMP.
3. Các loại thẩm định trong VMP
Trong VMP, các hoạt động thẩm định được phân loại rõ ràng nhằm đảm bảo kiểm soát toàn diện mọi yếu tố ảnh hưởng đến chất lượng sản phẩm dược. Mỗi loại thẩm định có vai trò riêng nhưng đều liên kết chặt chẽ, tạo thành một hệ thống kiểm soát đồng bộ từ thiết kế đến vận hành thực tế.
Trước hết là Qualification (thẩm định thiết bị), bao gồm bốn giai đoạn chính: DQ, IQ, OQ và PQ.
- DQ (Design Qualification - thẩm định thiết kế) là bước đầu tiên, nhằm xác nhận rằng thiết kế của thiết bị hoặc hệ thống đáp ứng đúng yêu cầu kỹ thuật và tiêu chuẩn GMP.
- IQ (Installation Qualification - thẩm định lắp đặt) kiểm tra việc lắp đặt thiết bị có đúng theo bản vẽ, tài liệu kỹ thuật và hướng dẫn của nhà sản xuất hay không.
- OQ (Operational Qualification - thẩm định vận hành) đánh giá khả năng hoạt động của thiết bị trong các điều kiện vận hành khác nhau, đảm bảo thiết bị hoạt động ổn định theo thông số đã thiết lập.
- PQ (Performance Qualification - thẩm định hiệu suất) xác nhận thiết bị hoặc hệ thống có thể vận hành ổn định trong điều kiện thực tế và đáp ứng yêu cầu sản xuất.
Xem thêm: Thẩm định IQ/OQ/PQ - những lỗi audit thường hay bắt lỗi
Bên cạnh thẩm định thiết bị, Process Validation (thẩm định quy trình sản xuất) là một trong những nội dung quan trọng nhất trong VMP. Mục tiêu của hoạt động này là chứng minh rằng quy trình sản xuất có thể tạo ra sản phẩm đạt chất lượng ổn định và nhất quán qua nhiều lô sản xuất. Điều này bao gồm việc xác định các thông số quan trọng (critical process parameters) và kiểm soát chúng trong giới hạn cho phép. Process Validation không chỉ giúp đảm bảo chất lượng mà còn giảm thiểu rủi ro sai lệch trong sản xuất.

Cleaning Validation (thẩm định làm sạch) tập trung vào việc đảm bảo các thiết bị và bề mặt tiếp xúc với sản phẩm được làm sạch hiệu quả, không để lại dư lượng hóa chất hoặc hoạt chất có thể gây nhiễm chéo. Đây là yêu cầu bắt buộc trong sản xuất dược phẩm, đặc biệt khi cùng một thiết bị được sử dụng cho nhiều sản phẩm khác nhau. Thẩm định làm sạch thường bao gồm việc xác định giới hạn chấp nhận (acceptance criteria) và phương pháp kiểm tra dư lượng.
HVAC Validation (thẩm định hệ thống HVAC) là một phần không thể thiếu trong nhà máy dược, vì hệ thống này ảnh hưởng trực tiếp đến môi trường phòng sạch. Hoạt động thẩm định HVAC bao gồm kiểm tra nhiệt độ, độ ẩm, áp suất, tốc độ gió và hiệu suất lọc HEPA. Ngoài ra, các thử nghiệm như Smoke Test và PAO Test cũng được thực hiện để đảm bảo luồng khí vận hành đúng thiết kế và không gây nhiễm bẩn. Các đơn vị như Thiết bị phòng sạch VCR thường cung cấp thiết bị và hỗ trợ kỹ thuật trong các hoạt động thẩm định này, giúp đảm bảo hệ thống đạt chuẩn GMP.
Utility Validation (thẩm định hệ thống tiện ích) bao gồm các hệ thống hỗ trợ như nước tinh khiết (PW - Purified Water), nước tiêm (WFI - Water for Injection), khí nén, hơi sạch và các hệ thống năng lượng khác. Những hệ thống này không trực tiếp tạo ra sản phẩm nhưng có ảnh hưởng lớn đến chất lượng. Việc thẩm định nhằm đảm bảo rằng các tiện ích luôn cung cấp đầu ra ổn định, đáp ứng tiêu chuẩn và không gây nhiễm bẩn.
Trong bối cảnh chuyển đổi số, Computer System Validation (CSV - thẩm định hệ thống máy tính) ngày càng trở nên quan trọng. CSV đảm bảo rằng các phần mềm, hệ thống điều khiển và quản lý dữ liệu hoạt động chính xác, đáng tin cậy và bảo mật. Điều này đặc biệt quan trọng trong việc lưu trữ và truy xuất dữ liệu sản xuất, đảm bảo tính toàn vẹn dữ liệu (data integrity) theo yêu cầu của GMP.
Nhìn chung, các loại thẩm định trong VMP không tồn tại độc lập mà có mối liên hệ chặt chẽ với nhau. Qualification đảm bảo thiết bị và hệ thống sẵn sàng, Process Validation đảm bảo quy trình ổn định, trong khi các hoạt động như HVAC, Cleaning và Utility Validation tạo nền tảng môi trường và điều kiện vận hành phù hợp. Sự kết hợp của tất cả các yếu tố này giúp nhà máy dược vận hành hiệu quả, đảm bảo chất lượng sản phẩm và đáp ứng đầy đủ các yêu cầu của GMP.
4. Quy trình xây dựng Validation Master Plan
Xây dựng Validation Master Plan (VMP) là một quá trình mang tính chiến lược, đòi hỏi sự phối hợp giữa nhiều bộ phận và sự hiểu biết sâu về hệ thống nhà máy dược. Một VMP hiệu quả không chỉ đáp ứng yêu cầu GMP mà còn giúp tối ưu hóa nguồn lực, giảm rủi ro và đảm bảo tính nhất quán trong toàn bộ hoạt động thẩm định. Để đạt được điều này, quy trình xây dựng VMP cần được thực hiện theo các bước rõ ràng và có hệ thống.
Bước đầu tiên là thu thập thông tin và đánh giá hiện trạng nhà máy. Đây là giai đoạn nền tảng nhằm hiểu rõ cấu trúc, hệ thống và mức độ hoàn thiện của cơ sở sản xuất. Các thông tin cần thu thập bao gồm sơ đồ nhà máy, danh mục thiết bị, hệ thống HVAC, hệ thống tiện ích và các quy trình sản xuất. Ngoài ra, cần đánh giá mức độ tuân thủ hiện tại so với yêu cầu GMP để xác định khoảng cách (gap analysis). Việc đánh giá chính xác hiện trạng giúp định hướng đúng cho các bước tiếp theo.
Sau khi có đầy đủ thông tin, bước tiếp theo là xác định phạm vi và mức độ thẩm định. Không phải tất cả các hệ thống đều cần thẩm định ở cùng một mức độ, do đó cần áp dụng phương pháp tiếp cận dựa trên rủi ro (risk-based approach) để xác định những hạng mục quan trọng nhất. Ví dụ, các hệ thống ảnh hưởng trực tiếp đến chất lượng sản phẩm như quy trình sản xuất, hệ thống HVAC, nước tinh khiết sẽ được ưu tiên thẩm định toàn diện. Việc xác định đúng phạm vi giúp tối ưu nguồn lực và tránh lãng phí.
Tiếp theo là thiết lập chiến lược validation phù hợp. Chiến lược này bao gồm việc lựa chọn phương pháp thẩm định, xác định trình tự thực hiện và mức độ chi tiết cho từng hạng mục. Một chiến lược hiệu quả cần đảm bảo tính logic, đồng bộ giữa các hoạt động như qualification (thẩm định thiết bị), process validation (thẩm định quy trình) và các hệ thống hỗ trợ. Đồng thời, chiến lược cũng cần phù hợp với quy mô nhà máy và định hướng phát triển trong tương lai.

Bước quan trọng tiếp theo là xây dựng timeline và phân bổ nguồn lực. Đây là giai đoạn chuyển kế hoạch thành hành động cụ thể. Timeline cần xác định rõ thứ tự thực hiện các hoạt động thẩm định, các mốc quan trọng (milestones) và thời gian hoàn thành. Song song đó, cần phân bổ nguồn lực bao gồm nhân sự, thiết bị và ngân sách. Việc lập kế hoạch hợp lý sẽ giúp tránh tình trạng chậm tiến độ hoặc thiếu hụt nguồn lực trong quá trình triển khai.
Sau khi đã có đầy đủ định hướng và kế hoạch, bước tiếp theo là soạn thảo tài liệu VMP. Tài liệu này cần được trình bày rõ ràng, đầy đủ các nội dung như phạm vi, chính sách, danh mục thẩm định, kế hoạch thực hiện và trách nhiệm của các bên liên quan. Ngoài ra, VMP cần được viết theo ngôn ngữ dễ hiểu nhưng vẫn đảm bảo tính kỹ thuật và tuân thủ yêu cầu GMP. Một tài liệu VMP tốt không chỉ phục vụ nội bộ mà còn phải sẵn sàng cho các đợt kiểm tra từ cơ quan quản lý.
Sau khi hoàn thành bản dự thảo, VMP cần được rà soát, phê duyệt và ban hành chính thức. Quá trình rà soát thường có sự tham gia của các bộ phận liên quan như QA, kỹ thuật và sản xuất để đảm bảo tính chính xác và khả thi. Sau khi được phê duyệt, VMP trở thành tài liệu chính thức và là cơ sở để triển khai các hoạt động thẩm định trong nhà máy.
Trong thực tế, có nhiều lỗi thường gặp khi xây dựng VMP mà doanh nghiệp cần tránh. Một trong những lỗi phổ biến là sao chép tài liệu từ các dự án khác mà không điều chỉnh phù hợp với thực tế, dẫn đến nội dung thiếu tính khả thi. Ngoài ra, việc xác định phạm vi không rõ ràng hoặc bỏ sót các hệ thống quan trọng cũng có thể gây rủi ro lớn. Một lỗi khác là thiếu sự phối hợp giữa các bộ phận, khiến kế hoạch không đồng bộ và khó triển khai. Cuối cùng, việc không cập nhật VMP khi có thay đổi trong hệ thống hoặc quy trình cũng làm giảm hiệu quả của tài liệu này.
Đặc biệt, trong quá trình xây dựng VMP, các hệ thống phòng sạch và HVAC cần được xem xét kỹ lưỡng vì đây là yếu tố ảnh hưởng trực tiếp đến môi trường sản xuất. Các hoạt động như Smoke Test, PAO Test cần được tích hợp vào kế hoạch thẩm định. Các đơn vị như Thiết bị phòng sạch VCR có thể hỗ trợ cung cấp thiết bị và tư vấn kỹ thuật, giúp đảm bảo các hạng mục này được triển khai đúng chuẩn và phù hợp với yêu cầu GMP.
Tóm lại, quy trình xây dựng VMP không chỉ là việc soạn thảo một tài liệu mà là quá trình hoạch định chiến lược toàn diện cho hoạt động thẩm định trong nhà máy dược. Việc thực hiện đúng và đầy đủ các bước sẽ giúp doanh nghiệp xây dựng nền tảng vững chắc, đảm bảo tuân thủ GMP và sẵn sàng cho mọi hoạt động kiểm tra, đánh giá trong tương lai.
Xem thêm: Quy trình thẩm định thiết bị phòng sạch theo GMP trong ngành dược phẩm
5. Yêu cầu GMP đối với Validation Master Plan
Trong ngành dược phẩm, Validation Master Plan (VMP) không chỉ là một tài liệu nội bộ mà còn là bằng chứng quan trọng để chứng minh sự tuân thủ GMP. Các hệ thống tiêu chuẩn như WHO GMP, EU GMP và PIC/S đều có những yêu cầu rõ ràng liên quan đến hoạt động thẩm định, trong đó VMP đóng vai trò trung tâm trong việc tổ chức và kiểm soát toàn bộ quá trình này.
Trước hết, các quy định từ WHO GMP, EU GMP và PIC/S đều nhấn mạnh rằng mọi hệ thống, thiết bị và quy trình có ảnh hưởng đến chất lượng sản phẩm phải được thẩm định và kiểm soát. Dù cách diễn đạt có thể khác nhau, nhưng điểm chung là yêu cầu doanh nghiệp phải có một kế hoạch tổng thể để quản lý các hoạt động validation. VMP chính là tài liệu đáp ứng yêu cầu đó, giúp doanh nghiệp chứng minh rằng các hoạt động thẩm định được thực hiện có hệ thống, có kế hoạch và tuân thủ nguyên tắc khoa học.
Một yêu cầu quan trọng khác là về tài liệu hóa (documentation). GMP yêu cầu mọi hoạt động thẩm định phải được ghi chép đầy đủ, rõ ràng và có thể kiểm tra lại. VMP cần mô tả chi tiết các phương pháp, phạm vi, trách nhiệm và kế hoạch thực hiện, đồng thời liên kết với các tài liệu liên quan như protocol (quy trình thẩm định) và report (báo cáo thẩm định). Việc tài liệu hóa đầy đủ không chỉ giúp kiểm soát nội bộ mà còn là cơ sở để chứng minh với cơ quan quản lý trong các đợt thanh tra.
Tính nhất quán và khả năng truy xuất dữ liệu cũng là yêu cầu cốt lõi trong GMP. Mọi thông tin liên quan đến thẩm định phải được lưu trữ và quản lý sao cho có thể truy xuất dễ dàng khi cần. Điều này bao gồm việc đảm bảo tính toàn vẹn dữ liệu (data integrity), tránh chỉnh sửa trái phép và duy trì lịch sử thay đổi rõ ràng. VMP cần thiết lập hệ thống quản lý tài liệu phù hợp để đảm bảo mọi dữ liệu liên quan đến validation đều được kiểm soát chặt chẽ.
Ngoài ra, GMP cũng yêu cầu VMP phải được cập nhật và duy trì liên tục. Nhà máy dược là một hệ thống động, có thể thay đổi về thiết bị, quy trình hoặc quy mô sản xuất. Mỗi khi có thay đổi, VMP cần được rà soát và điều chỉnh để phản ánh đúng hiện trạng. Việc không cập nhật VMP có thể dẫn đến sai lệch giữa tài liệu và thực tế, gây rủi ro trong quá trình vận hành và kiểm tra. Do đó, doanh nghiệp cần thiết lập quy trình kiểm soát thay đổi (change control) để đảm bảo VMP luôn phù hợp.

Trong các đợt thanh tra GMP, VMP thường là một trong những tài liệu được xem xét đầu tiên. Thanh tra viên sử dụng VMP để đánh giá cách doanh nghiệp tổ chức và kiểm soát hoạt động thẩm định. Một VMP rõ ràng, đầy đủ và cập nhật sẽ tạo ấn tượng tích cực, cho thấy doanh nghiệp có hệ thống quản lý chất lượng tốt và kiểm soát rủi ro hiệu quả. Ngược lại, nếu VMP thiếu sót hoặc không nhất quán, doanh nghiệp có thể bị đánh giá không tuân thủ, dẫn đến các yêu cầu khắc phục hoặc thậm chí ảnh hưởng đến giấy phép hoạt động.
Đặc biệt, các hệ thống quan trọng như HVAC và phòng sạch - yếu tố ảnh hưởng trực tiếp đến môi trường sản xuất - thường được chú ý trong quá trình thanh tra. Các hoạt động thẩm định liên quan như Smoke Test hoặc PAO Test cần được thể hiện rõ trong VMP. Các đơn vị như Thiết bị phòng sạch VCR có thể hỗ trợ cung cấp thiết bị và giải pháp phù hợp, giúp doanh nghiệp đảm bảo các yêu cầu kỹ thuật được đáp ứng và tích hợp đúng trong kế hoạch thẩm định.
Tóm lại, yêu cầu GMP đối với VMP không chỉ dừng lại ở việc “có tài liệu” mà còn đòi hỏi tài liệu đó phải đầy đủ, chính xác, nhất quán và luôn được cập nhật. Một VMP được xây dựng và duy trì tốt sẽ là nền tảng giúp doanh nghiệp đáp ứng các tiêu chuẩn quốc tế, giảm rủi ro và nâng cao hiệu quả vận hành trong dài hạn.
6. Ứng dụng VMP trong vận hành nhà máy dược
Validation Master Plan (VMP - Kế hoạch thẩm định tổng thể) không chỉ là tài liệu mang tính định hướng mà còn có vai trò thực tiễn rất lớn trong quá trình vận hành nhà máy dược. Khi được xây dựng và triển khai đúng cách, VMP trở thành công cụ giúp doanh nghiệp kiểm soát chất lượng, giảm thiểu rủi ro và đảm bảo hoạt động sản xuất luôn tuân thủ các tiêu chuẩn GMP.
Trước hết, VMP giúp kiểm soát chất lượng và giảm rủi ro một cách có hệ thống. Thông qua việc xác định rõ các hạng mục cần thẩm định và phương pháp kiểm soát, VMP giúp doanh nghiệp nhận diện các điểm có nguy cơ ảnh hưởng đến chất lượng sản phẩm. Các hoạt động như thẩm định thiết bị, quy trình sản xuất hay hệ thống môi trường đều được thực hiện theo kế hoạch, từ đó giảm thiểu sai sót và đảm bảo sản phẩm luôn đạt tiêu chuẩn. Đây là yếu tố đặc biệt quan trọng trong ngành dược, nơi mọi rủi ro đều có thể ảnh hưởng trực tiếp đến sức khỏe người dùng.
Một ứng dụng quan trọng khác của VMP là hỗ trợ các hoạt động audit (đánh giá nội bộ và bên ngoài). Trong các đợt kiểm tra GMP, VMP đóng vai trò như tài liệu tổng hợp, giúp thanh tra viên nhanh chóng hiểu được cách doanh nghiệp tổ chức và kiểm soát hoạt động thẩm định. Một VMP rõ ràng, đầy đủ sẽ giúp quá trình audit diễn ra thuận lợi hơn, giảm thiểu các câu hỏi hoặc yêu cầu bổ sung. Đồng thời, trong các đợt đánh giá nội bộ, VMP cũng là cơ sở để doanh nghiệp tự rà soát và cải tiến hệ thống.
VMP còn góp phần đảm bảo tính nhất quán trong sản xuất. Khi tất cả các thiết bị, quy trình và hệ thống đều được thẩm định và kiểm soát theo cùng một kế hoạch, doanh nghiệp có thể duy trì sự ổn định trong hoạt động sản xuất qua thời gian. Điều này giúp giảm biến động giữa các lô sản phẩm, đảm bảo chất lượng đồng đều và nâng cao uy tín của nhà máy trên thị trường.
Trong quá trình mở rộng hoặc nâng cấp nhà máy, VMP cũng thể hiện vai trò quan trọng. Khi có sự thay đổi về quy mô, thiết bị hoặc công nghệ, VMP sẽ là cơ sở để đánh giá lại các hoạt động thẩm định cần thực hiện. Điều này giúp doanh nghiệp triển khai các dự án mở rộng một cách có kiểm soát, đảm bảo các hệ thống mới được tích hợp đúng chuẩn và không ảnh hưởng đến hoạt động hiện tại. Việc có sẵn một VMP rõ ràng giúp tiết kiệm thời gian và chi phí khi thực hiện các thay đổi lớn.
Một yếu tố không thể bỏ qua là mối liên kết giữa VMP và hệ thống phòng sạch. Trong nhà máy dược, môi trường sản xuất đóng vai trò quyết định đến chất lượng sản phẩm. Các hệ thống như HVAC, lọc HEPA, kiểm soát áp suất và luồng khí đều cần được thẩm định và tích hợp trong VMP. Những hoạt động như Smoke Test hay PAO Test là minh chứng cho việc hệ thống phòng sạch hoạt động đúng thiết kế. Các đơn vị như Thiết bị phòng sạch VCR có thể hỗ trợ cung cấp thiết bị và giải pháp kỹ thuật, giúp đảm bảo các hạng mục liên quan đến môi trường được triển khai và kiểm soát hiệu quả trong khuôn khổ VMP.
Tóm lại, VMP không chỉ là tài liệu phục vụ kiểm tra mà còn là công cụ quản lý quan trọng trong vận hành nhà máy dược. Việc áp dụng VMP một cách hiệu quả sẽ giúp doanh nghiệp duy trì chất lượng ổn định, đáp ứng yêu cầu GMP và sẵn sàng thích ứng với các thay đổi trong tương lai.

7. Vai trò của hệ thống phòng sạch trong VMP
Trong nhà máy dược, hệ thống phòng sạch không chỉ là hạ tầng kỹ thuật mà còn là một phần cốt lõi trong Validation Master Plan (VMP - Kế hoạch thẩm định tổng thể). Mọi hoạt động thẩm định đều phải xem xét đến yếu tố môi trường, bởi đây là nơi trực tiếp ảnh hưởng đến chất lượng sản phẩm. Do đó, mối liên hệ giữa cleanroom và validation là không thể tách rời, đặc biệt trong các khu vực sản xuất vô trùng.
Phòng sạch đóng vai trò kiểm soát các yếu tố như hạt bụi, vi sinh, nhiệt độ, độ ẩm và áp suất - tất cả đều là những thông số quan trọng trong GMP. Trong VMP, các hệ thống liên quan đến phòng sạch phải được đưa vào danh mục thẩm định và kiểm soát chặt chẽ. Điều này đảm bảo rằng môi trường sản xuất luôn duy trì trong giới hạn cho phép và không gây ảnh hưởng đến sản phẩm.
Một trong những nội dung quan trọng là thẩm định hệ thống HVAC và HEPA. Hệ thống HVAC chịu trách nhiệm cung cấp và điều phối luồng khí, trong khi bộ lọc HEPA đảm bảo loại bỏ hạt bụi và vi sinh. Việc thẩm định bao gồm kiểm tra các thông số như lưu lượng khí, áp suất chênh lệch, tốc độ gió và hiệu suất lọc. Nếu các yếu tố này không đạt yêu cầu, toàn bộ hệ thống phòng sạch có thể bị ảnh hưởng.
Trong quá trình validation, các phương pháp như Smoke Test và PAO Test được sử dụng để đánh giá hiệu quả hoạt động của hệ thống. Smoke Test giúp quan sát trực quan luồng khí, đảm bảo dòng khí di chuyển đúng hướng và không tạo vùng nhiễu loạn. Trong khi đó, PAO Test giúp phát hiện các điểm rò rỉ trên bộ lọc HEPA, đảm bảo không có hạt ô nhiễm lọt qua. Hai phương pháp này thường được tích hợp trong VMP như các bước kiểm tra bắt buộc đối với hệ thống phòng sạch.
Trong thực tế, việc triển khai các hoạt động thẩm định liên quan đến phòng sạch đòi hỏi thiết bị chuyên dụng và chuyên môn kỹ thuật cao. Đây là lúc vai trò của các nhà cung cấp thiết bị trở nên quan trọng. Những đơn vị như Thiết bị phòng sạch VCR không chỉ cung cấp thiết bị đạt chuẩn mà còn hỗ trợ tư vấn giải pháp phù hợp với từng dự án. Từ việc lựa chọn hệ thống HVAC, bộ lọc HEPA đến triển khai các thử nghiệm như Smoke Test hay PAO Test, sự hỗ trợ từ các đơn vị chuyên nghiệp giúp đảm bảo các hạng mục được tích hợp đúng trong VMP và đáp ứng yêu cầu GMP.
Tóm lại, hệ thống phòng sạch là một trong những yếu tố trọng yếu trong VMP, đóng vai trò đảm bảo môi trường sản xuất đạt chuẩn và ổn định. Việc thẩm định và kiểm soát tốt hệ thống này không chỉ giúp đáp ứng yêu cầu pháp lý mà còn là nền tảng để đảm bảo chất lượng sản phẩm trong nhà máy dược.
8. Những lưu ý quan trọng khi xây dựng VMP
Khi xây dựng Validation Master Plan (VMP - Kế hoạch thẩm định tổng thể), doanh nghiệp cần chú ý đến nhiều yếu tố để đảm bảo tài liệu không chỉ đáp ứng yêu cầu GMP mà còn có thể triển khai hiệu quả trong thực tế. Một trong những nguyên tắc quan trọng nhất là đảm bảo tính thực tế và khả thi. VMP không nên chỉ mang tính lý thuyết hoặc sao chép từ tiêu chuẩn, mà cần phản ánh đúng điều kiện vận hành, nguồn lực và năng lực của nhà máy. Một kế hoạch quá phức tạp hoặc không phù hợp sẽ khó triển khai và dễ bị bỏ qua trong quá trình thực hiện.
Bên cạnh đó, VMP cần được xây dựng phù hợp với quy mô và loại hình sản xuất. Mỗi nhà máy dược có đặc thù riêng, từ sản xuất thuốc viên, thuốc tiêm đến sinh phẩm hoặc vaccine. Do đó, phạm vi và mức độ thẩm định cũng cần được điều chỉnh tương ứng. Ví dụ, các nhà máy sản xuất vô trùng sẽ yêu cầu thẩm định hệ thống phòng sạch và HVAC nghiêm ngặt hơn so với các nhà máy sản xuất thông thường.
Một yếu tố quan trọng khác là đảm bảo sự đồng bộ với hệ thống tài liệu GMP. VMP không tồn tại độc lập mà cần liên kết chặt chẽ với các tài liệu như SOP (Standard Operating Procedure - quy trình thao tác chuẩn), protocol và report. Sự đồng bộ này giúp đảm bảo tính nhất quán trong toàn bộ hệ thống chất lượng và tạo thuận lợi trong quá trình kiểm tra, đánh giá.
Doanh nghiệp cũng cần tránh việc sao chép máy móc VMP từ các dự án khác. Mặc dù có thể tham khảo cấu trúc hoặc nội dung, nhưng mỗi VMP cần được tùy chỉnh để phù hợp với điều kiện cụ thể của nhà máy. Việc sao chép mà không điều chỉnh có thể dẫn đến sai lệch giữa tài liệu và thực tế, gây rủi ro trong vận hành và khi audit GMP.

Cuối cùng, vai trò của đội ngũ chuyên môn là yếu tố quyết định đến chất lượng của VMP. Việc xây dựng tài liệu này đòi hỏi sự tham gia của nhiều bộ phận như QA, kỹ thuật, sản xuất và thậm chí là các chuyên gia bên ngoài. Đặc biệt, đối với các hệ thống quan trọng như phòng sạch và HVAC, sự hỗ trợ từ các đơn vị chuyên môn như Thiết bị phòng sạch VCR có thể giúp đảm bảo các yêu cầu kỹ thuật được tích hợp đúng và đầy đủ trong VMP. Một đội ngũ có kinh nghiệm sẽ giúp tài liệu không chỉ đúng chuẩn mà còn dễ triển khai và duy trì trong dài hạn.
9. FAQ - Câu hỏi thường gặp về Validation Master Plan
Trong quá trình xây dựng và triển khai Validation Master Plan (VMP - Kế hoạch thẩm định tổng thể), nhiều doanh nghiệp dược thường gặp các câu hỏi liên quan đến tính bắt buộc, cách áp dụng và các yêu cầu thực tế. Dưới đây là những thắc mắc phổ biến cùng giải đáp chi tiết.
- VMP có bắt buộc trong mọi nhà máy dược không?
Có. Theo các tiêu chuẩn GMP, mọi nhà máy dược đều cần có kế hoạch thẩm định tổng thể để kiểm soát các hệ thống ảnh hưởng đến chất lượng sản phẩm. Dù không phải lúc nào cũng được gọi tên cụ thể là “VMP” trong mọi tài liệu, nhưng về bản chất, một tài liệu tương đương là bắt buộc để chứng minh rằng các hoạt động validation được tổ chức và kiểm soát một cách có hệ thống.
- Khi nào cần xây dựng hoặc cập nhật VMP?
VMP cần được xây dựng ngay từ giai đoạn thiết kế hoặc chuẩn bị vận hành nhà máy. Sau đó, tài liệu này phải được cập nhật khi có thay đổi lớn như bổ sung thiết bị, thay đổi quy trình sản xuất, mở rộng nhà máy hoặc cập nhật tiêu chuẩn GMP. Ngoài ra, doanh nghiệp cũng nên rà soát định kỳ để đảm bảo VMP luôn phản ánh đúng thực trạng vận hành.
- VMP khác gì với Validation Protocol (quy trình thẩm định)?
VMP là tài liệu cấp chiến lược, mô tả tổng thể toàn bộ hoạt động thẩm định trong nhà máy. Trong khi đó, Validation Protocol là tài liệu chi tiết cho từng hoạt động cụ thể, ví dụ như thẩm định một thiết bị hoặc một quy trình. Có thể hiểu VMP là “kế hoạch tổng thể”, còn Protocol là “hướng dẫn thực hiện” cho từng phần trong kế hoạch đó.
- Bao lâu cần rà soát lại VMP?
Thông thường, VMP nên được rà soát ít nhất mỗi năm một lần hoặc theo chu kỳ thẩm định lại (re-validation - tái thẩm định). Tuy nhiên, nếu có bất kỳ thay đổi nào ảnh hưởng đến hệ thống hoặc quy trình, VMP cần được cập nhật ngay lập tức. Việc rà soát định kỳ giúp đảm bảo tài liệu luôn phù hợp và tránh sai lệch khi bị kiểm tra.
- Có thể thuê ngoài xây dựng VMP không?
Hoàn toàn có thể. Nhiều doanh nghiệp lựa chọn thuê các đơn vị tư vấn chuyên nghiệp để xây dựng VMP nhằm đảm bảo tính đầy đủ và tuân thủ GMP. Tuy nhiên, doanh nghiệp vẫn cần tham gia tích cực trong quá trình này để đảm bảo tài liệu phản ánh đúng thực tế vận hành. Việc kết hợp giữa chuyên gia bên ngoài và đội ngũ nội bộ sẽ mang lại hiệu quả tốt nhất.
- Những lỗi phổ biến khi bị audit GMP liên quan đến VMP là gì?
Một số lỗi thường gặp bao gồm: VMP không cập nhật theo thực tế, thiếu liên kết với các tài liệu khác, phạm vi thẩm định không đầy đủ hoặc không rõ ràng. Ngoài ra, việc sao chép tài liệu từ dự án khác mà không điều chỉnh cũng là lỗi phổ biến. Những sai sót này có thể khiến doanh nghiệp bị đánh giá không tuân thủ và yêu cầu khắc phục.
- VMP có liên quan gì đến hệ thống phòng sạch?
Hệ thống phòng sạch là một trong những yếu tố quan trọng nhất cần được đưa vào VMP. Các hoạt động thẩm định như HVAC Validation, Smoke Test và PAO Test đều liên quan trực tiếp đến môi trường sản xuất. Việc tích hợp đầy đủ các hạng mục này trong VMP giúp đảm bảo phòng sạch hoạt động đúng chuẩn và đáp ứng yêu cầu GMP. Các đơn vị như Thiết bị phòng sạch VCR có thể hỗ trợ cung cấp thiết bị và giải pháp, giúp doanh nghiệp triển khai các hoạt động thẩm định môi trường một cách hiệu quả và đúng tiêu chuẩn.
Những câu hỏi trên phản ánh các vấn đề cốt lõi khi xây dựng và áp dụng VMP trong thực tế. Việc hiểu rõ và triển khai đúng sẽ giúp doanh nghiệp nâng cao hiệu quả vận hành, giảm rủi ro và sẵn sàng cho các đợt kiểm tra GMP.
10. Kết luận
Validation Master Plan (VMP - Kế hoạch thẩm định tổng thể) là nền tảng cốt lõi trong hệ thống quản lý chất lượng của nhà máy dược. Không chỉ đóng vai trò định hướng cho toàn bộ hoạt động thẩm định, VMP còn giúp doanh nghiệp kiểm soát rủi ro, đảm bảo các hệ thống, thiết bị và quy trình luôn vận hành đúng thiết kế. Trong môi trường sản xuất dược phẩm, nơi mọi sai lệch đều có thể ảnh hưởng đến chất lượng và an toàn sản phẩm, vai trò của VMP càng trở nên quan trọng.
Bên cạnh đó, VMP là công cụ then chốt để đảm bảo tuân thủ GMP. Một VMP được xây dựng đầy đủ, rõ ràng và nhất quán sẽ giúp doanh nghiệp dễ dàng chứng minh với cơ quan quản lý rằng mọi hoạt động thẩm định đều được kiểm soát chặt chẽ. Đây cũng là yếu tố giúp quá trình audit và thanh tra diễn ra thuận lợi hơn.
Để đạt hiệu quả lâu dài, doanh nghiệp cần xây dựng VMP một cách bài bản, phù hợp với thực tế và đặc thù sản xuất. Đồng thời, việc cập nhật và duy trì VMP liên tục là điều bắt buộc nhằm đảm bảo tài liệu luôn phản ánh đúng hiện trạng hệ thống. Một VMP tốt không chỉ giúp đáp ứng tiêu chuẩn mà còn là công cụ hỗ trợ vận hành bền vững và nâng cao năng lực cạnh tranh của nhà máy dược.
Vietnam Cleanroom (VCR) là một doanh nghiệp hàng đầu tại Việt Nam chuyên cung cấp thiết bị và giải pháp phòng sạch. Với hơn 10 năm kinh nghiệm phục vụ các dự án phòng sạch đạt tiêu chuẩn GMP, VCR tự hào mang đến các thiết bị kỹ thuật cao như: đồng hồ chênh áp, khóa liên động, đèn phòng sạch, Pass Box, FFU (Fan Filter Unit), buồng cân, HEPA Box, Air Shower, cửa thép phòng sạch, tủ cách ly (ISOLATOR), và nhiều loại phụ kiện chuyên dụng khác
Không chỉ là nhà cung cấp thiết bị, VCR còn là đơn vị phân phối độc quyền các sản phẩm từ các thương hiệu quốc tế như LENGE và BLOCK Technical, đồng thời cung cấp các giải pháp phòng sạch toàn diện cho các lĩnh vực như dược phẩm, điện tử, y tế, thực phẩm và mỹ phẩm. VCR có đội ngũ chuyên gia giàu kinh nghiệm, kiến thức chuyên sâu về phòng sạch, hỗ trợ tư vấn về tiêu chuẩn, thiết kế, thi công và vận hành phòng sạch theo chuẩn ISO, GMP, HACCP, ISO 14644
VCR hướng đến trở thành thương hiệu quốc dân trong ngành phòng sạch, với mạng lưới cung ứng rộng khắp, VCR có các văn phòng tại Hà Nội, TP. HCM, đáp ứng mọi yêu cầu từ xây dựng đến nâng cấp môi trường sản xuất đạt chuẩn
Email: [email protected]
Điện thoại: (+84) 901239008
Địa chỉ:
VP Hà Nội: 9/675 Lạc Long Quân, P. Xuân La, Q. Tây Hồ, TP. Hà Nội
VP Hồ Chí Minh: 15/42 Phan Huy Ích, P.15, Q. Tân Bình, TP.HCM
Hãy liên hệ với VCR để tìm hiểu thêm về lĩnh vực phòng sạch hiệu quả nhất nhé!